Salute
Primo sì alla terapia genica con la Crispr

In Evidenza
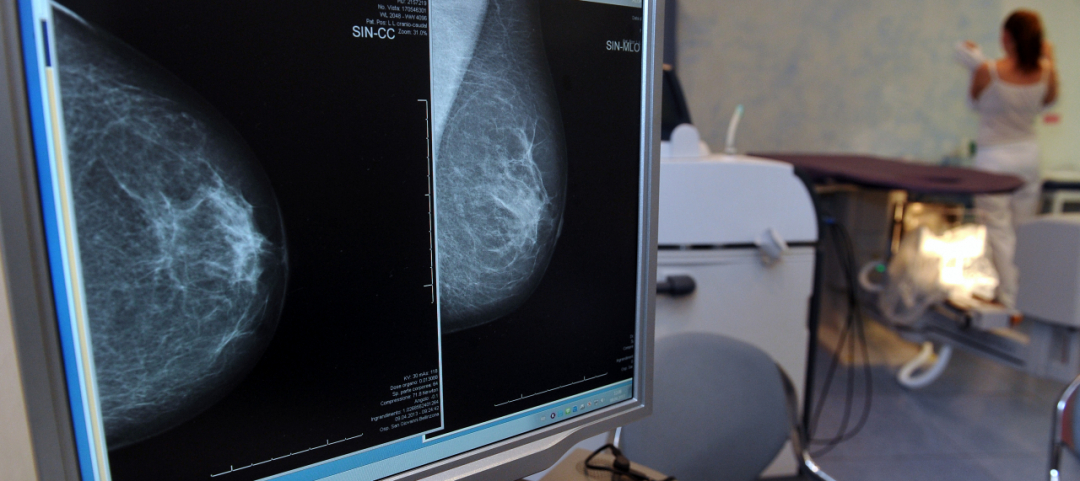
Tumore al seno, la biopsia liquida vede le recidive anni prima
Salute
Tumore polmone dei non fumatori, farmaco aumenta la sopravvivenza
Salute
Melanoma, lo studio del professor Ascierto: con la super-immunoterapia sopravvivenza al 72%
-

 Cronache5 anni fa
Cronache5 anni faVideo hard di una ragazzina di Avellino diffuso in rete, la polizia ha già denunciato tre minorenni ma “il giro è molto più largo”
-

 Cronache5 anni fa
Cronache5 anni faMorta a 24 anni dopo aver assunto per 2 mesi integratori. Gli esperti accusano Herbalife
-

 Cronache5 anni fa
Cronache5 anni faMattarella “revoca” la concessione ai Benetton che pagano i giornali per nascondere la notizia
-

 Cronache5 anni fa
Cronache5 anni faL’orrore dei video della decapitazione delle due ragazze scandinave in Marocco, i 4 arrestati avevano giurato fedeltà all’Isis
-

 Cronache5 anni fa
Cronache5 anni faOrrore in Marocco, il video della decapitazione di due giovani turiste scandinave a pochi chilometri da Marrakech pubblicato su Facebook: presi alcuni terroristi
-

 Cronache4 anni fa
Cronache4 anni faBoss di mafia liberi, Maresca minacciato: è finito tutto, sono stato lasciato solo, non ci sto più, vado a casa
-

 Cronache4 anni fa
Cronache4 anni faAlessandro Bologna alias Franchino il criminale, il boxer che fornisce ai ragazzi le “istruzioni” anti bulli
-

 Cronache4 anni fa
Cronache4 anni faCoronavirus, dopo Zagaria anche Cutolo tornerà a casa sua ad Ottaviano: hanno paura possa contagiarsi